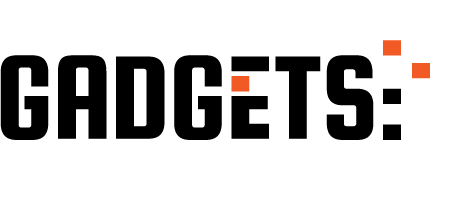
प्रोटीन वे वर्कहॉर्स हैं जो हमारी कोशिकाओं को चालू रखते हैं, और हमारी कोशिकाओं में कई हजारों प्रकार के प्रोटीन हैं, जिनमें से प्रत्येक एक विशेष कार्य करता है। शोधकर्ताओं ने लंबे समय से जाना है कि एक प्रोटीन की संरचना यह निर्धारित करती है कि यह क्या कर सकता है। हाल ही में, शोधकर्ताओं की सराहना करने के लिए आ रहे हैं कि एक प्रोटीन का स्थानीयकरण इसके कार्य के लिए भी महत्वपूर्ण है। कोशिकाएं डिब्बों से भरी होती हैं जो उनके कई डेनिज़ेंस को व्यवस्थित करने में मदद करती हैं। जीव विज्ञान की पाठ्यपुस्तकों के पृष्ठों को सुशोभित करने वाले प्रसिद्ध ऑर्गेनेल के साथ, इन रिक्त स्थानों में विभिन्न प्रकार के गतिशील, झिल्ली-कम डिब्बे भी शामिल हैं जो कुछ अणुओं को एक साथ साझा कार्यों को करने के लिए केंद्रित करते हैं। यह जानना कि एक दिया गया प्रोटीन कहाँ स्थानीयकृत करता है, और यह किसके साथ सह-स्थानीयकरण करता है, इसलिए बेहतर समझ के लिए उपयोगी हो सकता है कि प्रोटीन और स्वस्थ या रोगग्रस्त सेल में इसकी भूमिका, लेकिन शोधकर्ताओं के पास इस जानकारी की भविष्यवाणी करने के लिए एक व्यवस्थित तरीके का अभाव है।
इस बीच, प्रोटीन संरचना का आधे से अधिक सदी से अधिक के लिए अध्ययन किया गया है, कृत्रिम बुद्धिमत्ता उपकरण अल्फफोल्ड में समापन, जो एक प्रोटीन के अमीनो एसिड कोड से प्रोटीन संरचना की भविष्यवाणी कर सकता है, इसके भीतर बिल्डिंग ब्लॉकों की रैखिक स्ट्रिंग जो इसकी संरचना बनाने के लिए गुना होती है। Alphafold और मॉडल जैसे मॉडल अनुसंधान में व्यापक रूप से उपयोग किए जाने वाले उपकरण बन गए हैं।
प्रोटीन में अमीनो एसिड के क्षेत्र भी होते हैं जो एक निश्चित संरचना में नहीं बदलते हैं, लेकिन इसके बजाय सेल में गतिशील डिब्बों में शामिल होने में प्रोटीन में मदद करने के लिए महत्वपूर्ण हैं। MIT के प्रोफेसर रिचर्ड यंग और सहकर्मियों ने सोचा कि क्या उन क्षेत्रों में कोड का उपयोग प्रोटीन स्थानीयकरण की भविष्यवाणी करने के लिए किया जा सकता है, उसी तरह से कि अन्य क्षेत्रों का उपयोग संरचना की भविष्यवाणी करने के लिए किया जाता है। अन्य शोधकर्ताओं ने कुछ प्रोटीन अनुक्रमों की खोज की है जो प्रोटीन स्थानीयकरण के लिए कोड हैं, और कुछ ने प्रोटीन स्थानीयकरण के लिए भविष्य कहनेवाला मॉडल विकसित करना शुरू कर दिया है। हालांकि, शोधकर्ताओं को यह नहीं पता था कि किसी भी गतिशील डिब्बे के लिए एक प्रोटीन के स्थानीयकरण की भविष्यवाणी इसके अनुक्रम के आधार पर की जा सकती है, और न ही उनके पास स्थानीयकरण की भविष्यवाणी करने के लिए अल्फाफोल्ड के लिए एक तुलनीय उपकरण था।
अब, यंग, व्हाइटहेड इंस्टीट्यूट फॉर बायोलॉजिकल रिसर्च के सदस्य भी; यंग लैब पोस्टडॉक हेनरी किलगोर; रेजिना बारज़िले, स्कूल ऑफ इंजीनियरिंग ने एमआईटी के इलेक्ट्रिकल इंजीनियरिंग और कंप्यूटर विज्ञान और कंप्यूटर विज्ञान और कृत्रिम खुफिया प्रयोगशाला (CSAIL) में प्रिंसिपल अन्वेषक विभाग में एआई और हेल्थ के लिए प्रतिष्ठित प्रोफेसर; और सहकर्मियों ने ऐसा मॉडल बनाया है, जिसे वे PROTGP कहते हैं। जर्नल में 6 फरवरी को प्रकाशित एक पेपर में विज्ञानपहले लेखकों के साथ किलगोर और बारज़िले लैब स्नातक छात्रों के इटमार चिन, पीटर मिखाइल, और इलान मितनिकोव, क्रॉस-डिसिप्लिनरी टीम ने अपने मॉडल की शुरुआत की। शोधकर्ता बताते हैं कि PROTGP यह अनुमान लगा सकते हैं कि 12 ज्ञात प्रकार के डिब्बों में से कौन सा प्रोटीन स्थानीयकरण करेगा, साथ ही साथ एक रोग से जुड़े उत्परिवर्तन उस स्थानीयकरण को बदल देगा। इसके अतिरिक्त, अनुसंधान टीम ने एक सामान्य एल्गोरिथ्म विकसित किया जो विशिष्ट डिब्बों को स्थानीय बनाने के लिए उपन्यास प्रोटीन को डिजाइन कर सकता है।
“मेरी आशा है कि यह एक शक्तिशाली मंच की ओर एक पहला कदम है जो प्रोटीन का अध्ययन करने वाले लोगों को अपने शोध करने में सक्षम बनाता है,” यंग कहते हैं, “और यह हमें यह समझने में मदद करता है कि कैसे मनुष्य जटिल जीवों में विकसित होते हैं, वे कैसे हैं, कैसे उन प्राकृतिक प्रक्रियाओं को बाधित करते हैं, और एक कोशिका में शिथिलता का इलाज करने के लिए चिकित्सीय परिकल्पना और डिजाइन दवाओं को कैसे उत्पन्न करें।”
शोधकर्ताओं ने कोशिकाओं में प्रयोगात्मक परीक्षणों के साथ मॉडल की कई भविष्यवाणियों को भी मान्य किया।
“यह वास्तव में मुझे उत्साहित करता है कि मुझे लैब में इन चीजों को आज़माने के लिए कम्प्यूटेशनल डिजाइन से जाने में सक्षम होना चाहिए,” बारज़िले कहते हैं। “एआई के इस क्षेत्र में बहुत सारे रोमांचक कागजात हैं, लेकिन 99.9 प्रतिशत उन लोगों में से कभी भी वास्तविक प्रणालियों में परीक्षण नहीं किया जाता है। युवा प्रयोगशाला के साथ हमारे सहयोग के लिए धन्यवाद, हम परीक्षण करने में सक्षम थे, और वास्तव में सीखते हैं कि हमारा एल्गोरिथ्म कितना अच्छा कर रहा है।”
मॉडल विकसित करना
शोधकर्ताओं ने ज्ञात स्थानीयकरण के साथ प्रोटीन के दो बैचों पर PROTGPs को प्रशिक्षित और परीक्षण किया। उन्होंने पाया कि यह सही ढंग से भविष्यवाणी कर सकता है कि प्रोटीन उच्च सटीकता के साथ कहां समाप्त होते हैं। शोधकर्ताओं ने यह भी परीक्षण किया कि प्रोटीन एक प्रोटीन के भीतर रोग से जुड़े म्यूटेशन के आधार पर प्रोटीन स्थानीयकरण में परिवर्तन की भविष्यवाणी कैसे कर सकता है। कई उत्परिवर्तन – एक जीन और उसके संबंधित प्रोटीन के लिए अनुक्रम में परिवर्तन – एसोसिएशन के अध्ययन के आधार पर बीमारी का योगदान या कारण में पाया गया है, लेकिन जिन तरीकों से उत्परिवर्तन रोग के लक्षणों को जन्म देते हैं वे अज्ञात रहते हैं।
यह पता लगाना कि एक उत्परिवर्तन कैसे बीमारी में योगदान देता है, इसके लिए तंत्र महत्वपूर्ण है क्योंकि तब शोधकर्ता उस तंत्र को ठीक करने, बीमारी को रोकने या इलाज करने के लिए चिकित्सा विकसित कर सकते हैं। युवा और सहकर्मियों को संदेह था कि कई रोग से जुड़े उत्परिवर्तन प्रोटीन स्थानीयकरण को बदलकर बीमारी में योगदान कर सकते हैं। उदाहरण के लिए, एक उत्परिवर्तन एक प्रोटीन को आवश्यक भागीदारों वाले डिब्बे में शामिल होने में असमर्थ बना सकता है।
उन्होंने रोग से जुड़े म्यूटेशन के साथ 200,000 से अधिक प्रोटीनों को खिलाकर इस परिकल्पना का परीक्षण किया, और फिर यह दोनों से यह पूछने के लिए कि उन उत्परिवर्तित प्रोटीनों को स्थानीयकृत करने और मापने के लिए यह पूछने के लिए कि किसी दिए गए प्रोटीन के लिए सामान्य से उत्परिवर्तित संस्करण में कितना बदल गया है। भविष्यवाणी में एक बड़ी पारी स्थानीयकरण में संभावित परिवर्तन को इंगित करती है।
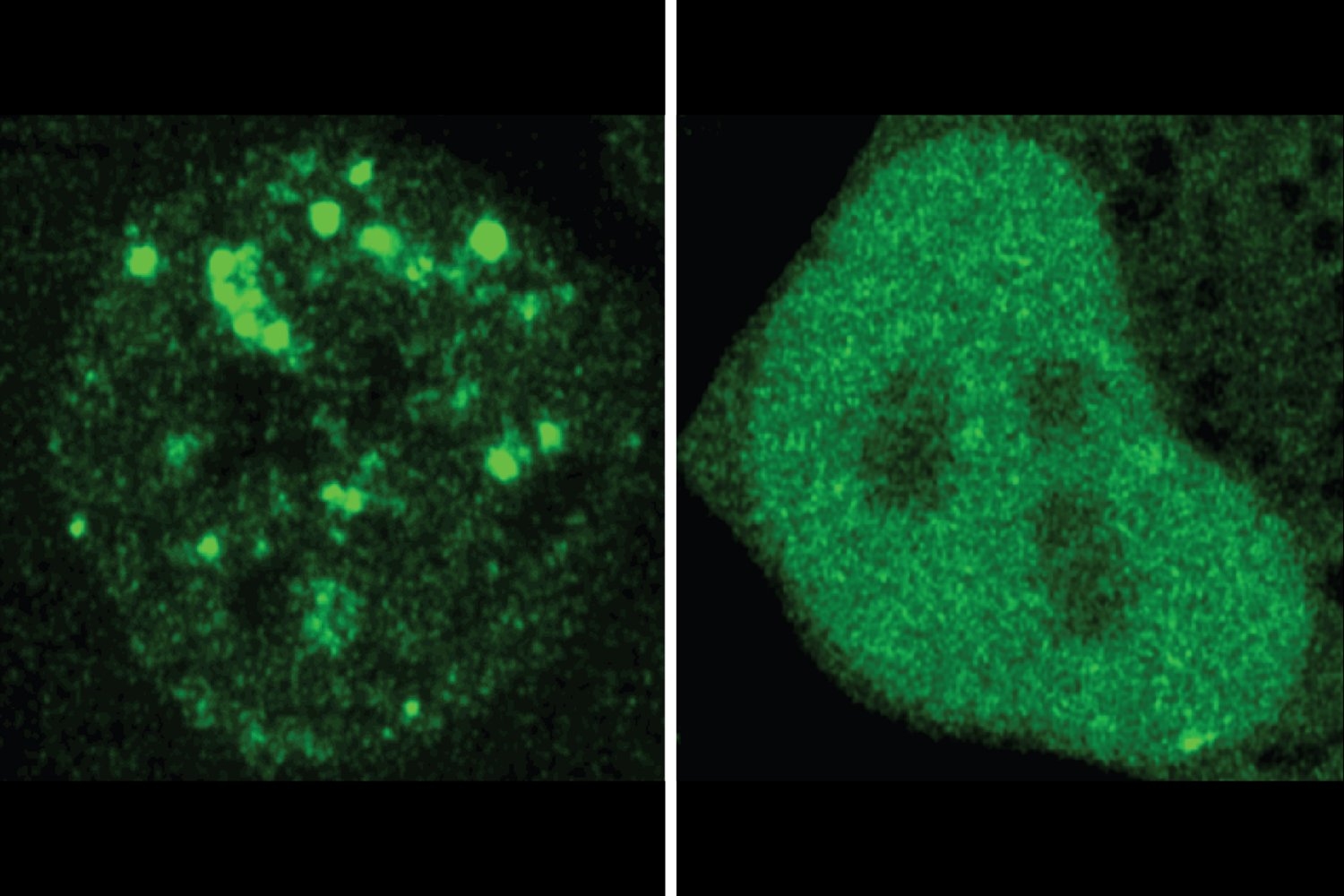
शोधकर्ताओं ने कई मामले पाए जिनमें एक रोग से जुड़े उत्परिवर्तन एक प्रोटीन के स्थानीयकरण को बदलने के लिए दिखाई दिया। उन्होंने कोशिकाओं में 20 उदाहरणों का परीक्षण किया, जहां कोशिका में एक सामान्य प्रोटीन और इसका उत्परिवर्तित संस्करण समाप्त हो गया, की तुलना करने के लिए प्रतिदीप्ति का उपयोग करते हुए। प्रयोगों ने PROTGP की भविष्यवाणियों की पुष्टि की। कुल मिलाकर, निष्कर्ष शोधकर्ताओं के संदेह का समर्थन करते हैं कि गलत-स्थानीयकरण रोग का एक कमतर तंत्र हो सकता है, और रोग को समझने और नए चिकित्सीय मार्गों की पहचान करने के लिए एक उपकरण के रूप में PROTGP के मूल्य को प्रदर्शित करता है।
“सेल एक ऐसी जटिल प्रणाली है, जिसमें कई घटकों और बातचीत के जटिल नेटवर्क हैं,” मितनिकोव कहते हैं। “यह सोचना बहुत दिलचस्प है कि इस दृष्टिकोण के साथ, हम सिस्टम को गड़बड़ कर सकते हैं, उस के परिणाम को देख सकते हैं, और इसलिए सेल में तंत्र की खोज को ड्राइव कर सकते हैं, या यहां तक कि उसके आधार पर चिकित्सीय विकसित करते हैं।”
शोधकर्ताओं को उम्मीद है कि अन्य लोग उसी तरह से PROTGPs का उपयोग करना शुरू करते हैं जैसे कि वे Alphafold जैसे पूर्वानुमान संरचनात्मक मॉडल का उपयोग करते हैं, प्रोटीन फ़ंक्शन, शिथिलता और बीमारी पर विभिन्न परियोजनाओं को आगे बढ़ाते हैं।
उपन्यास पीढ़ी के लिए भविष्यवाणी से परे चल रहा है
शोधकर्ता अपने भविष्यवाणी मॉडल के संभावित उपयोगों के बारे में उत्साहित थे, लेकिन वे यह भी चाहते थे कि उनका मॉडल मौजूदा प्रोटीन के स्थानीयकरण की भविष्यवाणी करने से परे जाए, और उन्हें पूरी तरह से नए प्रोटीन डिजाइन करने की अनुमति दे। लक्ष्य मॉडल के लिए पूरी तरह से नए अमीनो एसिड अनुक्रम बनाने के लिए था, जो एक सेल में गठित होने पर, एक वांछित स्थान पर स्थानीयकरण करेगा। एक उपन्यास प्रोटीन उत्पन्न करना जो वास्तव में एक फ़ंक्शन को पूरा कर सकता है – इस मामले में, एक विशिष्ट सेलुलर डिब्बे में स्थानीयकरण का कार्य – अविश्वसनीय रूप से मुश्किल है। अपने मॉडल की सफलता की संभावना में सुधार करने के लिए, शोधकर्ताओं ने अपने एल्गोरिथ्म को केवल प्रकृति में पाए जाने वाले प्रोटीन डिजाइन करने के लिए विवश किया। यह एक दृष्टिकोण है जो आमतौर पर दवा डिजाइन में उपयोग किया जाता है, तार्किक कारणों से; प्रकृति को यह पता लगाने के लिए अरबों साल हैं कि कौन से प्रोटीन अनुक्रम अच्छी तरह से काम करते हैं और कौन सा नहीं।
यंग लैब के साथ सहयोग के कारण, मशीन लर्निंग टीम यह परीक्षण करने में सक्षम थी कि क्या उनके प्रोटीन जनरेटर ने काम किया है। मॉडल के अच्छे परिणाम थे। एक दौर में, इसने न्यूक्लियोलस को स्थानीय बनाने के लिए 10 प्रोटीन उत्पन्न किए। जब शोधकर्ताओं ने सेल में इन प्रोटीनों का परीक्षण किया, तो उन्होंने पाया कि उनमें से चार ने न्यूक्लियोलस के लिए दृढ़ता से स्थानीय किया, और अन्य लोगों को उस स्थान की ओर भी मामूली पूर्वाग्रह हो सकते हैं।
“हमारी प्रयोगशालाओं के बीच सहयोग हम सभी के लिए इतना उदार रहा है,” मिखाइल कहते हैं। “हमने सीखा है कि एक -दूसरे की भाषाओं को कैसे बोलना है, हमारे मामले में बहुत कुछ पता चला है कि कोशिकाएं कैसे काम करती हैं, और प्रयोगात्मक रूप से हमारे मॉडल का परीक्षण करने का मौका होने से, हम यह पता लगाने में सक्षम हैं कि हमें वास्तव में मॉडल काम करने के लिए क्या करने की आवश्यकता है, और फिर इसे बेहतर काम करने के लिए।”
इस तरह से कार्यात्मक प्रोटीन उत्पन्न करने में सक्षम होने से शोधकर्ताओं की चिकित्सा को विकसित करने की क्षमता में सुधार हो सकता है। उदाहरण के लिए, यदि किसी दवा को एक लक्ष्य के साथ बातचीत करनी चाहिए जो एक निश्चित डिब्बे के भीतर स्थानीयकृत करता है, तो शोधकर्ता इस मॉडल का उपयोग एक दवा को डिजाइन करने के लिए भी कर सकते हैं। इससे दवा को अधिक प्रभावी बनाना चाहिए और दुष्प्रभावों को कम करना चाहिए, क्योंकि दवा अपने लक्ष्य के साथ संलग्न होने और अन्य अणुओं के साथ बातचीत करने में कम समय बिताएगी, जिससे ऑफ-टारगेट प्रभाव पैदा होगा।
मशीन लर्निंग टीम के सदस्य स्थानीयकरण से परे अन्य कार्यों के साथ उपन्यास प्रोटीन को डिजाइन करने के लिए इस सहयोग से जो कुछ भी सीखा है, उसका उपयोग करने की संभावना के बारे में उत्साहित हैं, जो चिकित्सीय डिजाइन और अन्य अनुप्रयोगों के लिए संभावनाओं का विस्तार करेगा।
“बहुत सारे कागजात दिखाते हैं कि वे एक प्रोटीन डिजाइन कर सकते हैं जो एक सेल में व्यक्त किया जा सकता है, लेकिन ऐसा नहीं है कि प्रोटीन का एक विशेष कार्य है,” चिन कहते हैं। “हमारे पास वास्तव में कार्यात्मक प्रोटीन डिजाइन था, और अन्य जनरेटिव मॉडल की तुलना में अपेक्षाकृत विशाल सफलता दर थी। यह वास्तव में हमारे लिए रोमांचक है, और कुछ ऐसा जो हम बनाना चाहते हैं।”
इसमें शामिल सभी शोधकर्ता PROTGP को एक रोमांचक शुरुआत के रूप में देखते हैं। वे अनुमान लगाते हैं कि उनके उपकरण का उपयोग प्रोटीन फ़ंक्शन में स्थानीयकरण की भूमिकाओं और बीमारी में गलत स्थानीयकरण की भूमिकाओं के बारे में अधिक जानने के लिए किया जाएगा। इसके अलावा, वे अधिक प्रकार के डिब्बों को शामिल करने, अधिक चिकित्सीय परिकल्पनाओं का परीक्षण करने और उपचारों या अन्य अनुप्रयोगों के लिए तेजी से कार्यात्मक प्रोटीन डिजाइन करने के लिए मॉडल के स्थानीयकरण भविष्यवाणियों का विस्तार करने में रुचि रखते हैं।
“अब जब हम जानते हैं कि स्थानीयकरण के लिए यह प्रोटीन कोड मौजूद है, और मशीन लर्निंग मॉडल उस कोड की समझ बना सकते हैं और यहां तक कि इसके तर्क का उपयोग करके कार्यात्मक प्रोटीन बना सकते हैं, जो इतने सारे संभावित अध्ययनों और अनुप्रयोगों के लिए दरवाजा खोलता है,” किलगोर कहते हैं।
(टैगस्टोट्रांसलेट) एमआईटी व्हाइटहेड इंस्टीट्यूट (टी) एमआईटी सीएसएएल (टी) प्रोटीन स्थानीयकरण (टी) प्रोटीन संरचनाएं (टी) प्रोटीन कार्यक्षमता (टी) अल्फाफोल्ड (टी) अमीनो एसिड (टी) रोग उत्परिवर्तन (टी) रोग (टी) प्रोटग्प (टी) रिचर्ड यंग (टी) रेजिना बारज़िलाय (टी) हेनरी क्लेर (टी) मिखाइल (टी) इलान मितनिकोव